研究内容
私たちは、けがや病気などで失われた生体組織を再生するための細胞足場材料、幹細胞の機能を制御するための材料、およびがんを治療するための複合材料に関する研究を行っています。細胞足場材料として、生体吸収性合成高分子および天然高分子を用いて多孔質構造や力学強度、細胞親和性などを制御した高分子多孔質材料および複合多孔質材料を開発し、これらの細胞足場材料を用いた組織再生について研究しています。また、組織再生で重要となる幹細胞の機能を制御するため、細胞を内包したハイドロゲル、機能性分子をマイクロパターン化した材料、生体内の微小環境を模倣した細胞培養材料についても研究を行っています。さらに、組織再生効果に加えてがん殺傷効果も示す複合材料に関する研究にも取り組んでいます。
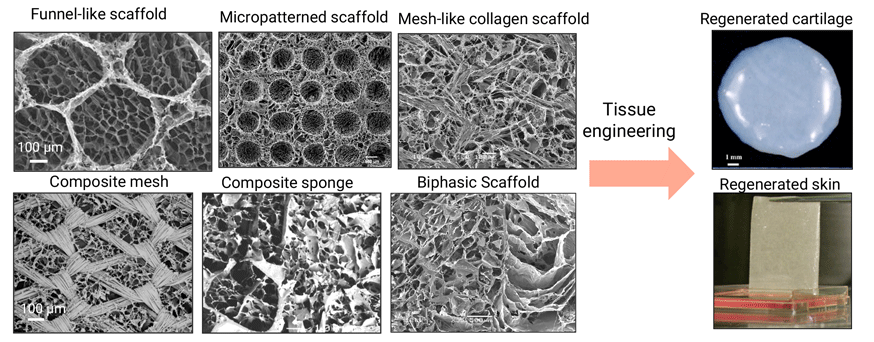
1.再生医療のための細胞足場材料の開発
細胞足場材料は、細胞の接着・増殖・分化などの機能を制御し、生体組織の再生を誘導するきわめて重要な役割を果たします。細胞足場材料には、細胞の支持体として必要な力学強度を持つことに加え、生体吸収性や細胞親和性も求められます。私たちは、生体吸収性合成高分子のメッシュやスポンジなどに天然高分子や生理活性因子を複合化することで、力学特性、細胞親和性ともに優れた細胞足場材料を開発しました。また、氷微粒子を空孔の鋳型に用い、連通した多孔質構造をもつ細胞足場材料を開発しました。この手法を応用し、氷鋳型の配置を制御することによって、空孔をパターン状に配列させた細胞足場材料も開発しました。これらの細胞足場材料を用いて皮膚や軟骨、骨、筋肉などの組織の再生を行っています。
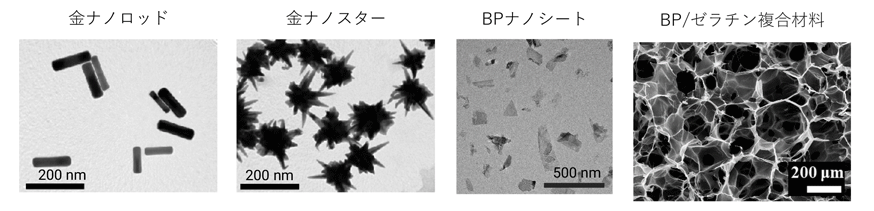
2.組織再生とがん治療のための高次機能性複合足場材料の開発
外科手術によるがん治療は広く行われていますが、病巣を切除した後も体内にがん細胞が残存している場合があります。また、組織を切除することによって、臓器や体の機能が失われてしまうことがあります。これらの問題を解決するために、私たちは、残存したがん細胞を死滅させるとともに、切除によって欠損した組織の再生も必要であると考えました。がん細胞が正常細胞に比べて熱に弱いことに着目し、近赤外光の照射や交流磁場の印加によって発熱するナノ粒子を細胞足場材料に複合化するというコンセプトを掲げました。この複合足場材料を患部に移植した後、外部から近赤外光を照射したり、交流磁場を印加したりすると、発生する熱でがん細胞を殺傷することができます。がん細胞が死滅した後、足場材料は欠損部位の組織再生を誘導します。これまで、金ナノ粒子、黒リンナノシート、磁性酸化鉄ナノ粒子などをコラーゲンやゼラチンの多孔質体に導入した複合足場材料を開発してきました。
3.生体模倣型足場材料の開発
生体内では細胞外マトリックスは細胞を取り囲み、細胞機能の調節に関わっています。細胞外マトリックスの組成は、細胞や組織の種類によって異なるだけではなく、組織発生プロセスにおいてダイナミックに変化しています。私たちは、細胞培養技術と脱細胞化技術を融合し、このダイナミックに変化する細胞外マトリックスを模倣した材料を創出しました。組織発生の各段階を模倣した「組織分化模倣型」マトリックス足場材料、生体親和性に優れた「自家細胞由来」マトリックス足場材料を開発し、幹細胞の分化制御や組織再生への応用をはかっています。

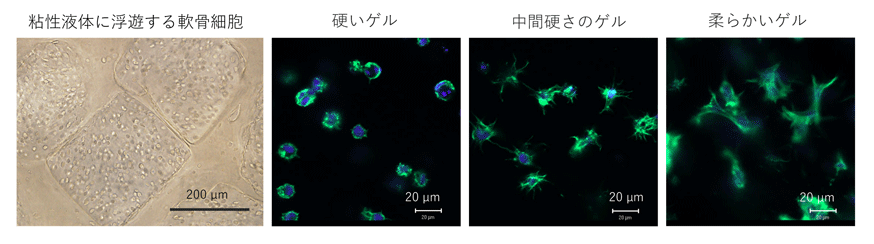
4.三次元細胞培養用ハイドロゲルの開発
細胞は周囲の微小環境から力学刺激シグナルを受け取り、様々な組織を形成します。私たちは、細胞足場材料の粘弾性が細胞の機能にどのような影響を与えるかを明らかにするため、ハイドロゲルを用いた三次元培養システムを開発しました。具体的にはまず、ゼラチンにメタクリロイル基を導入することによって、メタクリロイル化ゼラチンマクロマーを合成し、次に光重合によりゲル化させます。ゼラチンハイドロゲルに細胞を内包した状態や粘性液体の細胞懸濁液を内包した状態で三次元培養を行い、ハイドロゲルの硬さや液体の粘性の違いが細胞機能にどのように影響を及ぼすかを研究しています。
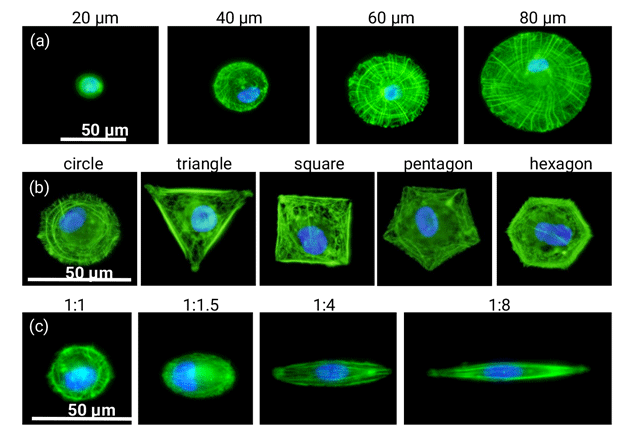
5.細胞機能を制御するためのマイクロパターン材料の開発
細胞の大きさや形状は、組織や臓器の種類によって多種多様であり、組織・臓器の構造や機能に深く関わっています。細胞の大きさや形状などの物理的ファクターを人工的に制御するために、マイクロパターン状の細胞接着領域をもつ表面を用いて細胞をパターニングし、細胞の接着、増殖、分化などの機能に与える影響が研究されています。私たちは、光リソグラフィー法を用いて機能性高分子や生理活性物質をマイクロパターン化した材料を開発し、幹細胞の機能制御を行っています。これまで、細胞の大きさ、形状、伸展、キラリティー、細胞間相互作用の制御により、幹細胞のメカニクス、ステムネス、分化、遺伝子導入効率にどのような影響が生じるかを明らかにしました。