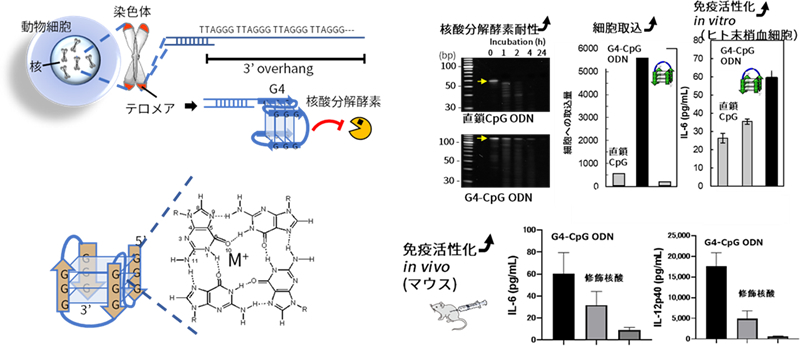
DNA高次構造の改変による核酸ナノメディシンの機能制御(山崎担当)
自然免疫受容体のトール様受容体9(TLR9) はCG配列を含む非メチル化一本鎖DNA(CpG ODN)と結合し免疫を活性化します。TLR9は結合するCpG ODNの立体構造によって、誘導するサイトカインが異なります。我々は、この現象を解明するためにグアニン四重鎖構造を用いてCpG ODNの形成する高次構造を制御し、細胞内での動態を解明することを進めています。得られた情報をもとに、新しいCpG ODNの開発を進めています。
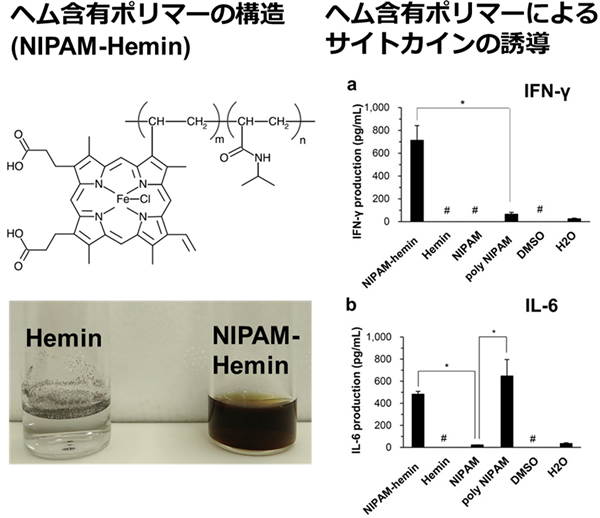
マラリア原虫の生産するヘモゾインを模倣した免疫活性化剤の開発(山崎担当)
マラリア原虫が生産するヘモゾインが免疫活性化能を示すことが報告されています。我々はヘモゾインのヘム集合構造に着目し、ヘムから構成されるポリマーを開発し、このポリマーがヒト免疫細胞において抗体産出を誘導するインターフェロンγとインターロイキン6を誘導することを報告しました。現在ヘム含有ポリマーが免疫を活性化する機構の解明を進めており、またワクチンアジュバンドへの応用を目指して研究を進めています。
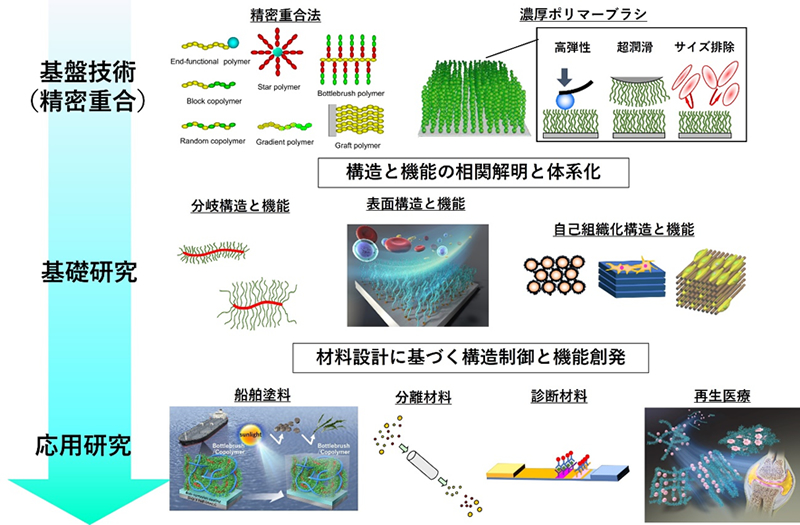
精密重合法を用いた高分子の構造制御(吉川担当)
精密重合法を駆使した高分子材料設計による、新規生体材料の創出を行っています。具体的には、重合の最適化と高分子の構造制御、高次構造と機能の相関解明などの基盤研究を行い、生体機能を自在に制御できる高分子材料の開発に取り組んでいます。
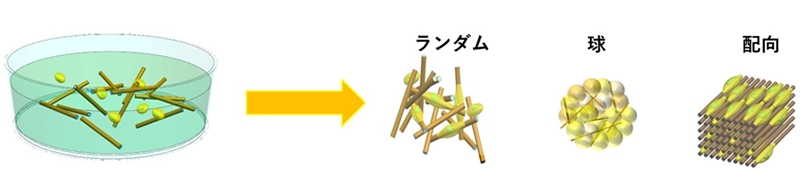
ナノ繊維を用いた細胞の自己組織化 (吉川担当)
セルロースナノファイバーや電解紡糸ファイバーなどのナノ繊維を用いた足場材料の開発を行っています。興味深いことに、ナノ繊維は化学組成や構造特性に応じて、細胞と自己組織化し、ユニークな高次構造を形成します。現在、自己組織化のメカニズム解明に取り組むとともに、軟骨再生や心筋再生の研究を進めています。
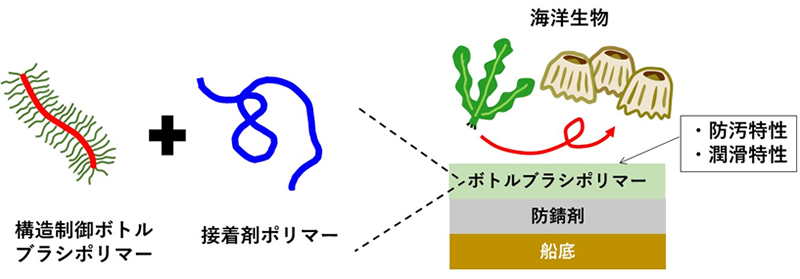
構造制御ボトルブラシポリマーを用いた船底塗料の開発 (吉川担当)
1本の主鎖からグラフト側鎖を伸ばした櫛形ポリマーは、側鎖のセグメント密度が高ければ濃厚ポリマーブラシと類似の性質(高弾性・超潤滑・生体適合性)を示すことが知られています。現在、このボトルブラシポリマーを用いて、防汚剤フリーで海洋生物付着を防止し得る、次世代船底塗料の開発に取り組んでいます。