
大学院生・ポスドク・外研生・インターンシップ生を
募集しています!
最先端のバイオマテリアル研究、特に再生医療や組織工学、ドラッグデリバリー分野に興味のある方はぜひご連絡ください。
バイオマテリアル研究を通して、世界で活躍できる人材育成を目指しています。
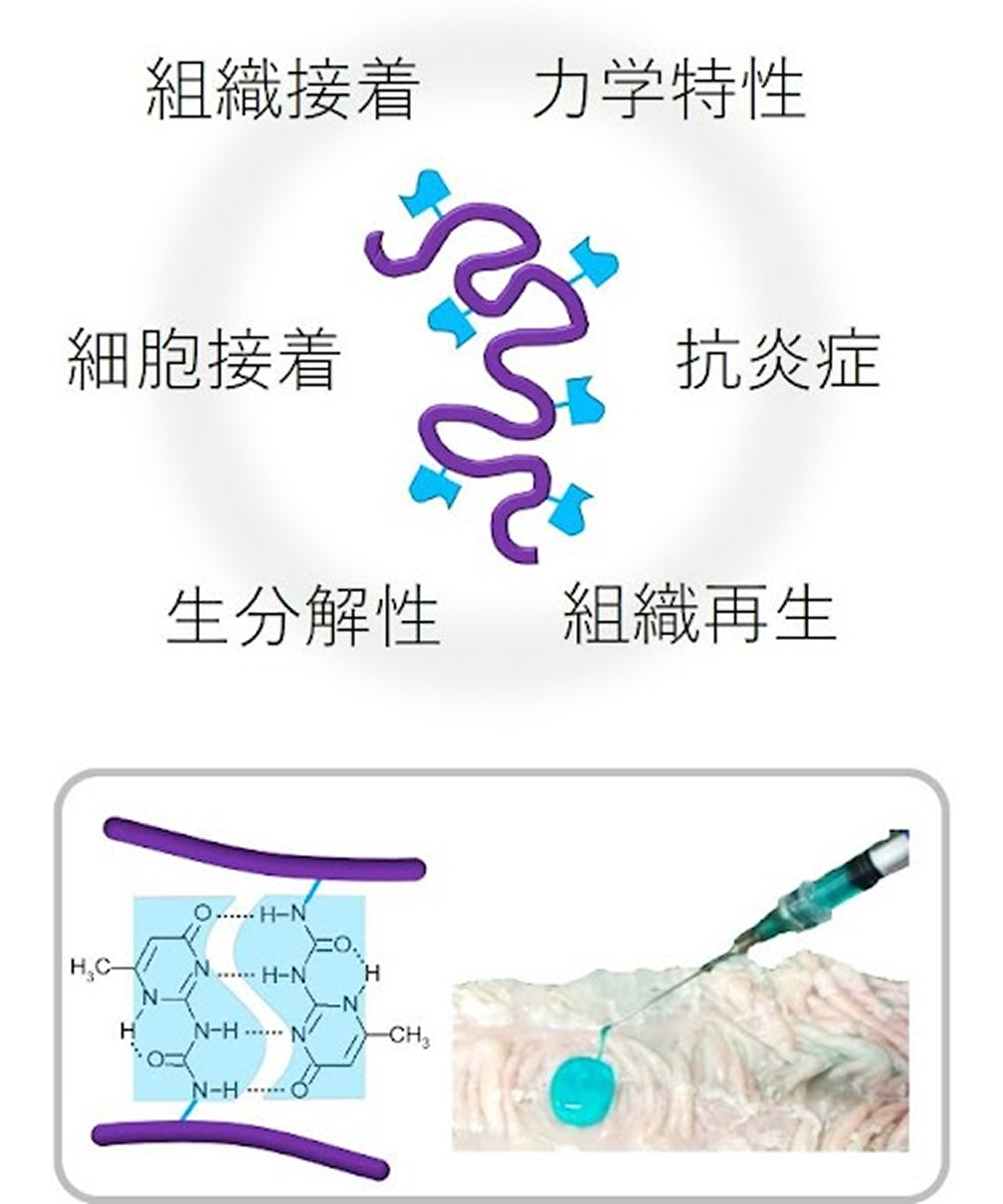
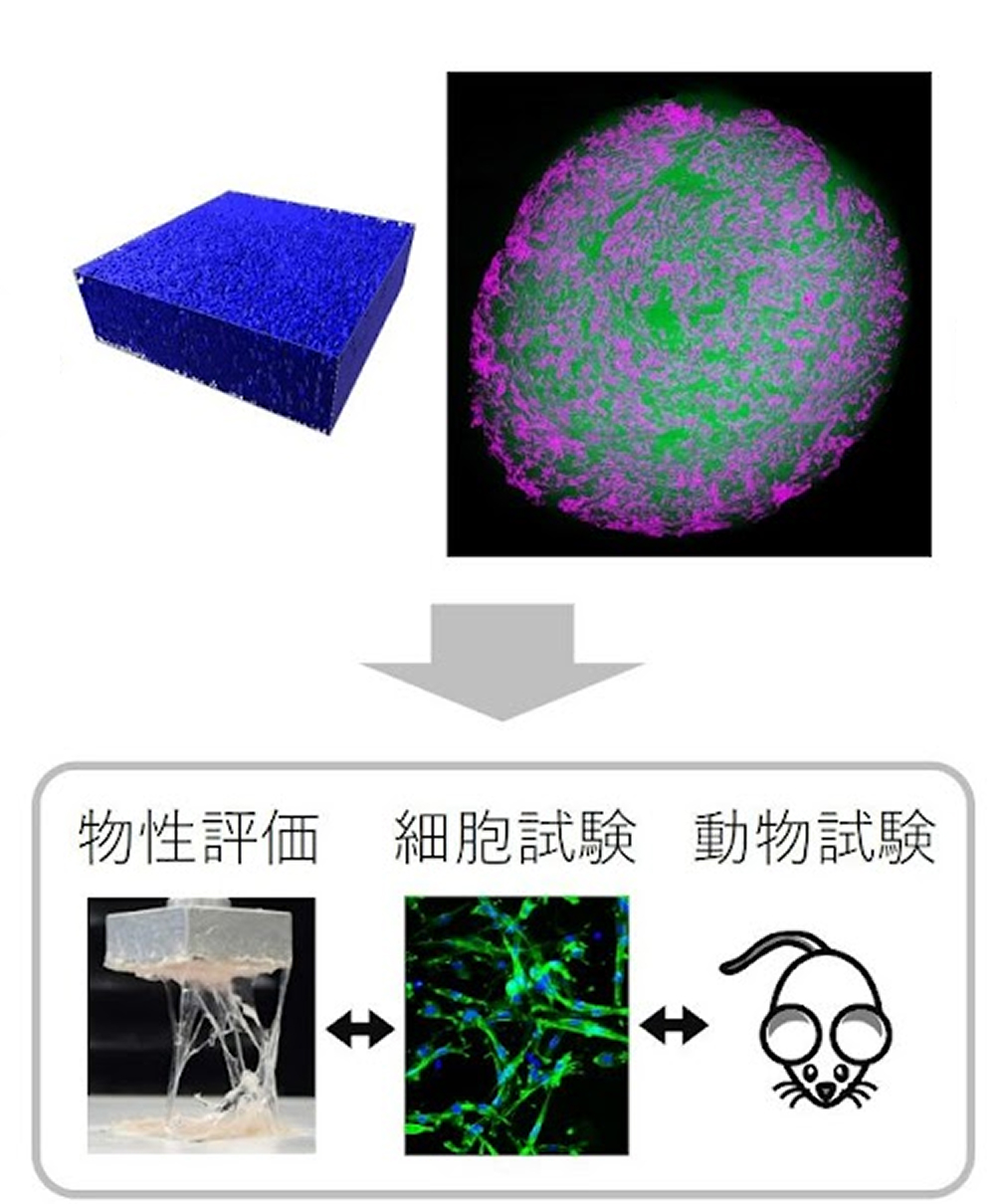
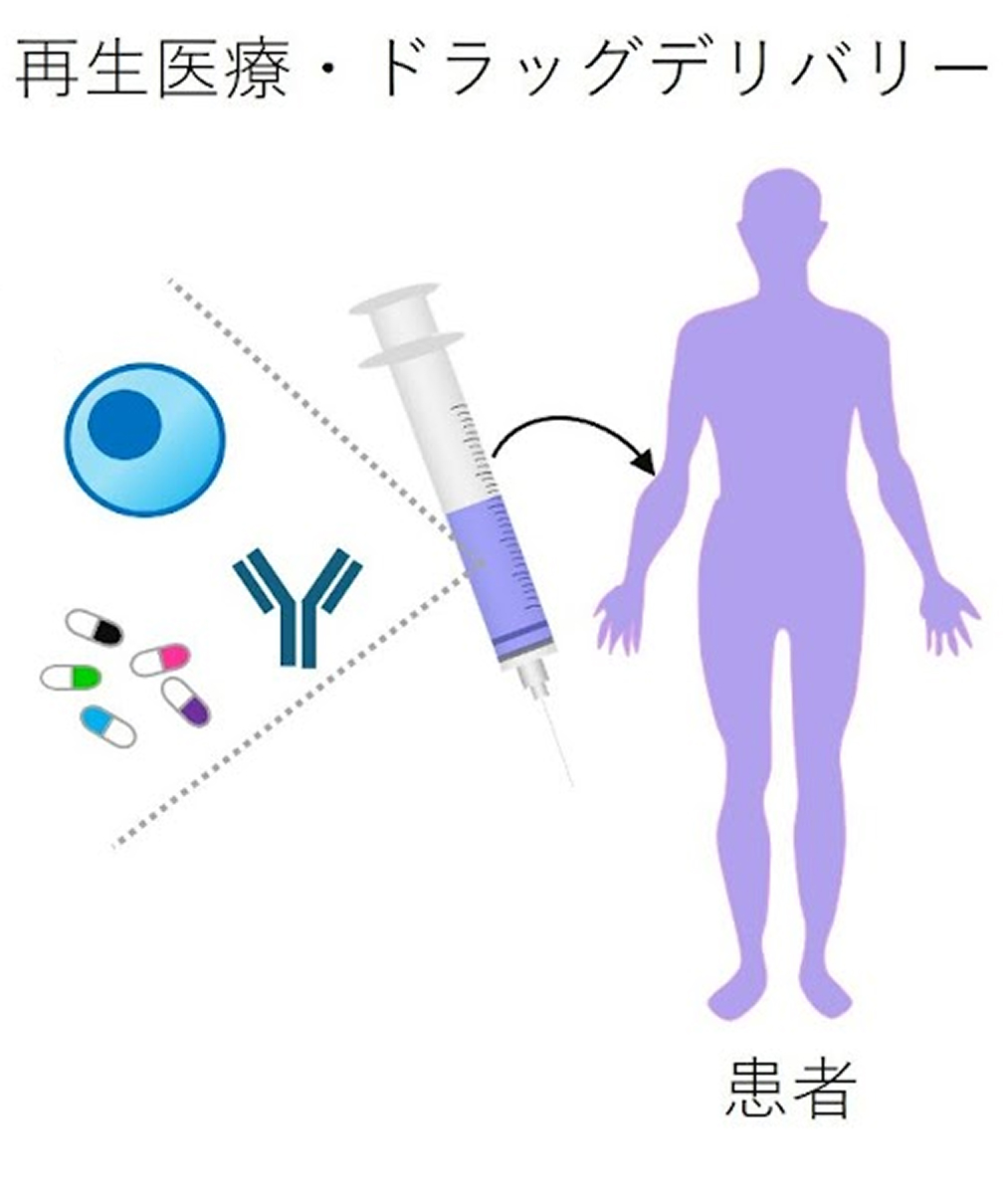
西口研究チームでは、傷ついた組織の再生を促進するバイオマテリアルの開発を行っています。具体的には、生体高分子の化学修飾や相分離制御技術を基盤として、機能性インジェクタブルゲルや3Dプリンティング技術、薬剤送達キャリアの開発を進めています。これらの技術は、再生医療や創薬への応用が期待できます。
- 研究分野
-
- 生体材料工学
- 生体医工学
- 高分子化学
- 再生医療
- 組織工学
- キーワード
-
- ハイドロゲル
- 相分離
- 組織再生
- 足場材料
- ドラッグデリバリー
Hydrogels for
Tissue Regeneration
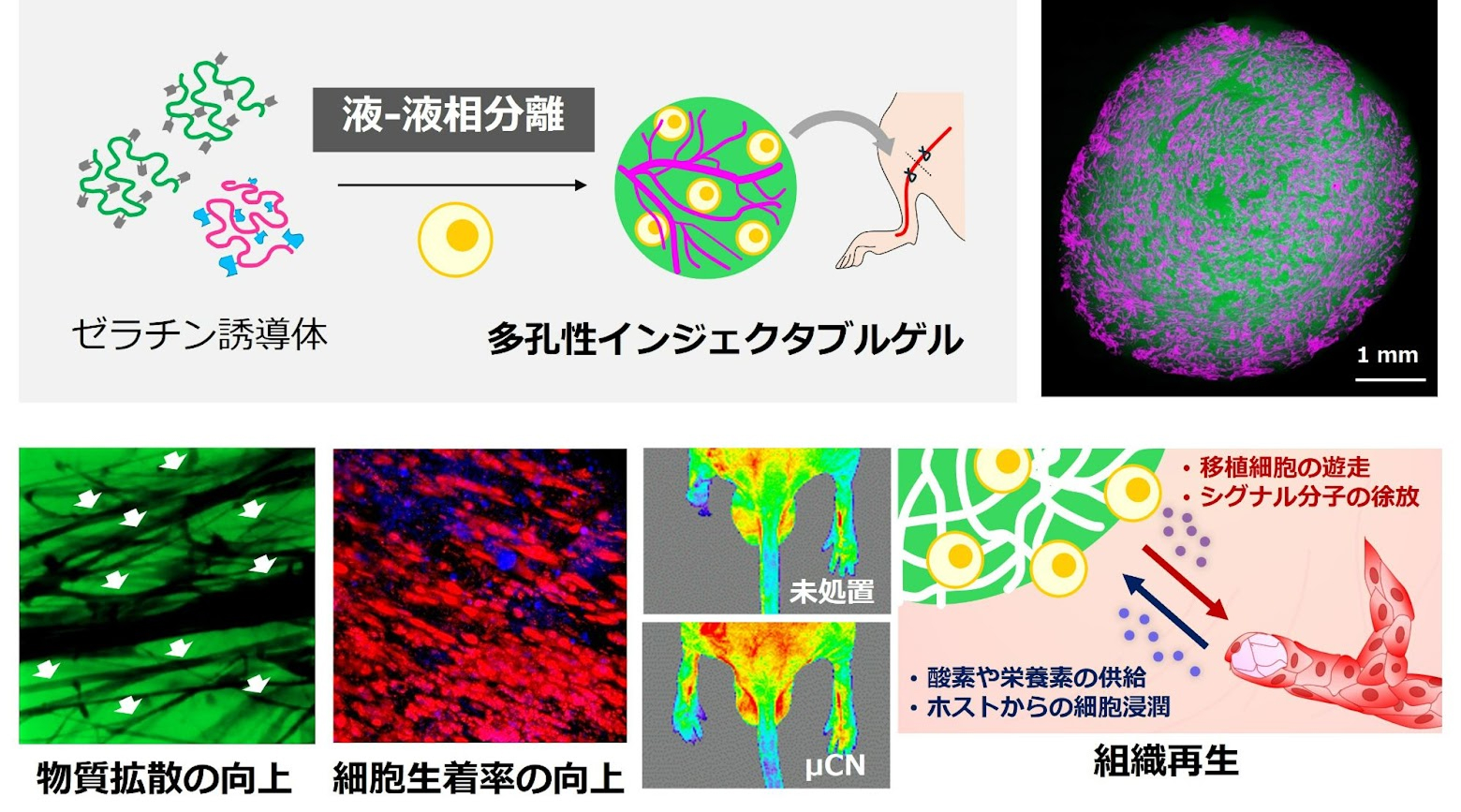
多孔性インジェクタブルゲルによる
細胞移植技術の開発と再生医療応用
(ゲル+細胞)
細胞移植治療では、細胞生着率の低さが課題となっています。我々は、液-液相分離制御技術を用いて、多孔性インジェクタブルゲルを設計し、細胞の生着率と生存率を向上させるための新しい材料を開発しました。本材料は、細胞移植の治療効果を向上させることができるため、再生医療への応用が期待できます。
Biomaterials 2024
Biomacromocromlecules 2024
Adv Funct Mater 2025

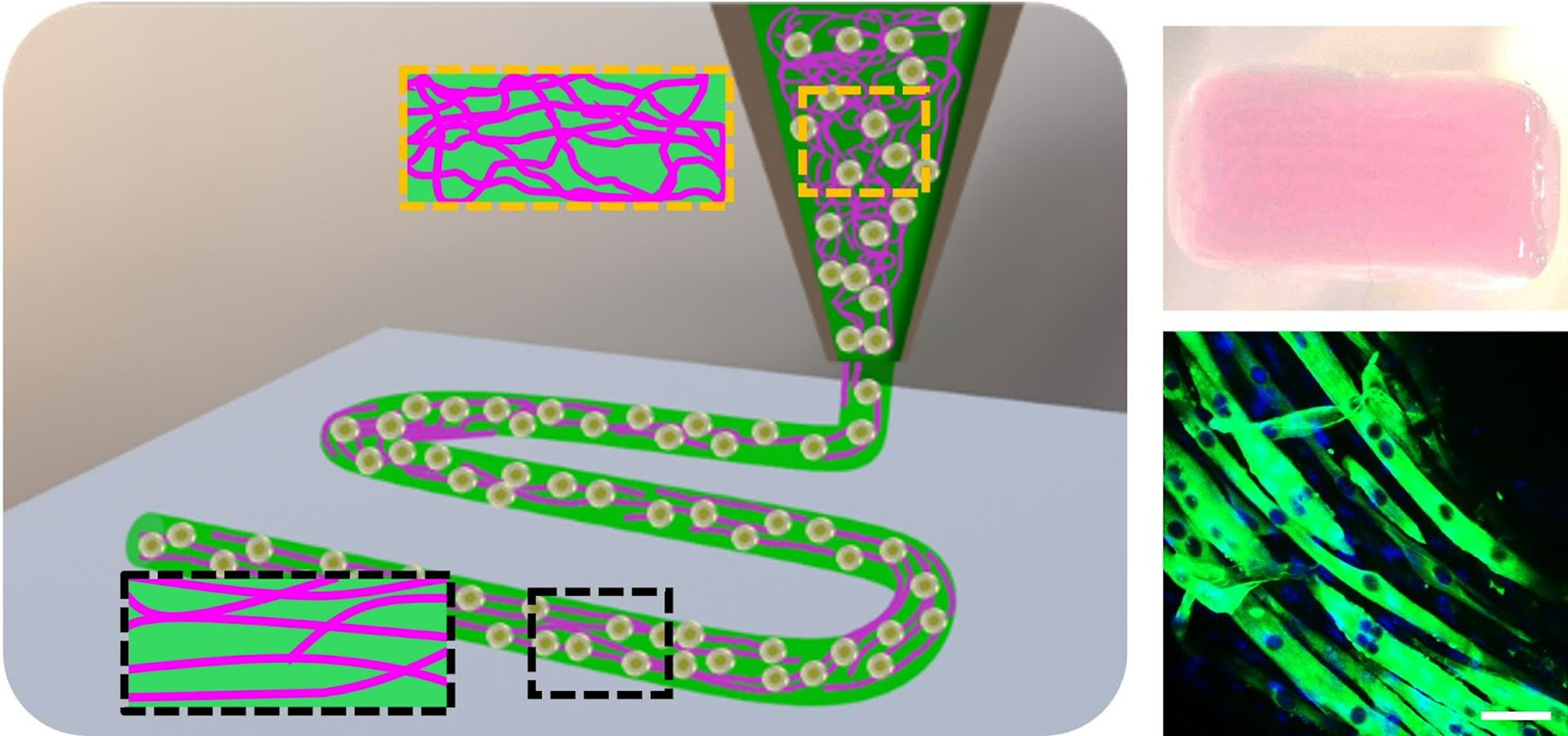
組織工学的アプローチによる
生体組織の3Dバイオプリンティング
(ゲル+細胞)
生体組織に類似した構造と機能を有する組織体の体外構築技術のひとつとして、3Dバイオプリンティングが近年注目されています。3Dバイオプリンターを用いることで、細胞の3D配置の自動制御ができ、立体的な臓器を生体外で高速構築できるため、再生医療や創薬モデルへの応用が期待されています。新たなバイオプリンティング用のインク(バイオインク)の設計に着目し、細胞の3D配向化と物質拡散の向上を可能とする多孔化バイオインクを開発しています。
Small 2026
インジェクタブルゲル・ナノ粒子を用いた
ドラッグデリバリー技術の開発
(ゲル+薬剤)
ドラッグデリバリーシステムとは、薬剤を必要な場所に必要な量だけ、適切なタイミングで届けるための技術です。インジェクタブルゲルやナノ粒子に薬剤を担持させて体に投与することで、薬効を最大限に高めながら副作用を抑えるドラッグデリバリーが可能となります。これらの技術は、がん治療や炎症性疾患治療に有用です。
Adv Funct Mater 2021
J Mater Chem B 2023
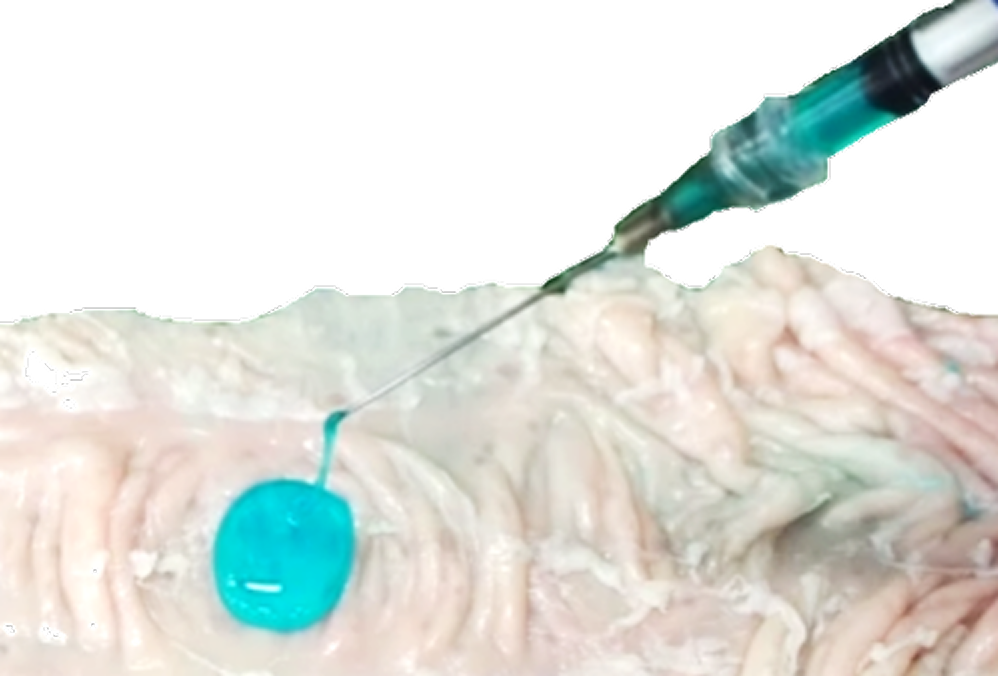
組織接着性足場材料による
組織再生技術の開発
(ゲルのみ)
術後合併症とは、手術中やその後に生じる合併症で、出血や癒着、炎症反応、感染などが発生してしまいます。我々は、このような術後合併症を予防するためのバイオマテリアルとして、インジェクタブルゲルを開発しています。目的に応じて適切な分子設計を行うことで、術後合併症を予防しながら、組織再生を促進する新しい医療材料を開発することを目指しています。
Acta Biomater 2021
Acta Biomater 2022
Acta Biomater 2025
Adv Healthc Mater 2025
Member

西口 昭広
主幹研究員
(Akihiro Nishiguchi, Ph.D.)
- 筑波大学大学院 理工情報生命学術院 数理物質系 准教授
- 東京理科大学 先進工学研究科 マテリアル創成工学専攻 客員准教授

安江 華
修士課程学生(M2)
(Hana Yasue)
- 東京理科大学大学院 先進工学研究科 マテリアル創成工学専攻
- 細胞移植用インジェクタブルゲルの開発を行っています。

大田 美穂
テクニカルスタッフ
Publications
Total publications: 72, h-index: 27, Total Citations: >2200
2026
- N. Otsuka, Y. Yagura, T. Inoue, T. Taguchi, A. Nishiguchi, H. Asahara, Enhancement of Cell Adhesion on 3D-Printed PLA through Surface Modification Using Photo-Activated Chlorine Dioxide, ACS Appl Biomater, in press (2026).
- S. Uehara, F. Sasaki*, H. Maeda, M. Hinokuchi, A. Tanaka, S. Arima, S. Hashimoto, H. Sahara, S. Kanmura, Y. Kobayashi, A. Nishiguchi, T. Taguchi, Sprayable hydrophobized gelatin microparticles prevent delayed gastric bleeding after endoscopic procedure in an anticoagulated swine model. Sci. Rep. In acceptance.
- D. Palai, H. Yasue, M. Ohta, K. Uto, T. Taguchi, A. Nishiguchi*, Oriented micropore-forming bioinks for 3D bioprinting of muscle tissues. Small 22, e09439 (2026).
- H. Nishino, S. Ito, H. Komatsu, Y. Kobayashi, S. Minamisakamoto, Y. Kobayashi, S. Watanabe, A. Nishiguchi, T. Taguchi*, Effect of crosslinking densities on decanoyl-group modified Alaska pollock gelatin microparticles as tissue-adhesive hemostatic powders. Biomater. Adv. 180, 214534 (2026).
2025
- M. Ohira, M. Kitamura, H. Iwasaki, H. Ohta-Okano, H. Tsujii, R. Nakamura, T. Nakazawa, A. Nishiguchi, M. Yamamoto, K. Osada, S. Toyooka, H. Cabral, A. Masamune, M. R. Kano*, H. Y. Tanaka*, Collagen Signaling via DDR1 Exacerbates Barriers to Macromolecular Drug Delivery in a 3D Model of Pancreatic Cancer Fibrosis. Small 21, e06926 (2025).
- A. Nishiguchi*, M. Ohta, D. Palai, H. Yasue, P. Sarkar, H. Komatsu, T. Taguchi*, Microporous tissue adhesive promotes cell infiltration and wound healing. Acta Biomater., 206, 215-224 (2025).
- H. Yasue, T. Taguchi, T. Asoh, A. Nishiguchi*, Cell-delivering injectable hydrogels with tunable microporous structures improve therapeutic efficacy for volumetric muscle loss. Adv. Funct. Mater. 35, e08278 (2025).
- S. Ito, H. Komatsu, S. Minamisakamoto, D. Palai, A. Nishiguchi, T. Taguchi*, Local administration of an anti-cancer drug using tissue adhesive microparticles based on hydrophobically modified Alaska pollock gelatin for post-surgical cancer chemotherapy. Colloids Surf. B: Biointerfaces 254, 114825 (2025).
- D. Palai, H. Yasue, S. Ito, H. Komatsu, T. Taguchi*, A. Nishiguchi*, Functionalization of viscoelastic gels with decellularized extracellular matrix microparticles enhances tissue adhesion, cell spreading, and tissue regeneration. Biomater. Sci. 13, 3576-3584 (2025).
- A. Nishiguchi*, M. Ohta, D. Palai, S. Ito, K. Mori, R. Akagi, C. Bajan, G. Lambard, K. Sodeyama, T. Taguchi*, In-situ forming supramolecular nanofiber hydrogel as a biodegradable liquid embolic agent for post-embolization tissue remodeling. Adv. Healthc. Mater. 14, 2403784 (2025).
- H. Yano, F. Sasaki*, H. Maeda, S. Uehara, M. Kabayama, Y. Fujino, A. Tanaka, M. Hinokuchi, S. Arima, S. Hashimoto, S. Kanmura, S. Ito, A. Nishiguchi, T. Taguchi, A. Ido, Effect of sprayable, highly adhesive hydrophobized gelatin microparticles on esophageal stenosis after endoscopic submucosal dissection: an experimental study in a swine model. Esophagus 22, 95-104 (2025).
- K. Nagasaka, H. Komatsu, S Ito, D. Palai, A. Nishiguchi, T. Taguchi*, Elevation and adhesion properties of injectable hydrogels based on catechol/boronic acid-modified Alaska pollock gelatin for endoscopic submucosal dissection. Colloids Surf. B: Biointerfaces 245, 114307 (2025).
2024
- A. Nishiguchi*, E. Araki, M. Ohta, D. Palai, S. Ito, T. Taguchi, Development of phase-separating microfiber network hydrogels to promote in vitro vascularization. Biomacromolecules 25, 6146-6154 (2024).
- A. Nishiguchi*, Advances in injectable hydrogels with biological and physicochemical functions for cell delivery. Polym. J. 56, 895–903 (2024).
- S Ito, K. Nagasaka, H. Komatsu, D. Palai, A. Nishiguchi, T. Taguchi*, Improved hydration property of tissue adhesive/hemostatic microparticle based on hydrophobically-modified Alaska pollock gelatin. Biomater. Adv. 159, 213834 (2024).
- D. Palai, M. Ohta, I. Cetnar, T. Taguchi*, A. Nishiguchi*, Enhanced ROS scavenging and tissue adhesive abilities in injectable hydrogels by protein modification with oligoethyleneimine. Biomater. Sci. 12, 2312-2320 (2024).
- A. Nishiguchi*, S. Ito, K. Nagasaka, H. Komatsu, K. Uto, T. Taguchi*, Injectable microcapillary network hydrogels engineered by liquid-liquid phase separation for stem cell transplantation. Biomaterials 305, 122451 (2024).
- S. Ito, K. Nagasaka, H. Komatsu, H. Mamiya, M. Takeguchi, A. Nishiguchi, T. Taguchi*, Sprayable tissue adhesive microparticle–magnetic nanoparticle composites for local cancer hyperthermia. Biomater. Adv. 156, 213707 (2024).
2023
- H. Komatsu, S. Watanabe, S. Ito, K. Nagasaka, A. Nishiguchi, T. Taguchi*, Improved swelling property of tissue adhesive hydrogels based on α-cyclodextrin/decyl group-modified Alaska pollock gelatin inclusion complexes. Macromol. Biosci. 23, 2300097 (2023).
- A. Nishiguchi*, T. Taguchi, Inflammation-targeting polyamine nanomedicines for the treatment of ulcerative colitis. J. Mater. Chem. B., 11, 4005-4013 (2023).
- A. Nishiguchi*, S. Ito, K. Nagasaka, T. Taguchi*, Tissue-adhesive decellularized extracellular matrix patches reinforced by supramolecular gelator to repair abdominal wall defects. Biomacromolecules, 24, 1545-1554 (2023).
- M. Kabayama, F. Sasaki*, H. Maeda, Y. Fujino, H. Yano, A. Tanaka, S. Arima, S. Tanoue, S. Hashimoto, S. Kanmura, H. Hirade, A. Nishiguchi, T. Taguchi, A. Ido, Effects of sprayable, highly-adhesive hydrophobized gelatin microparticles on endoscopic submucosal dissection: a swine model. Digestion, 104, 137-147 (2023).
- S. Ito, A. Nishiguchi, T. Taguchi*, Effect of particle size on the tissue adhesion and particle floatation for a colloidal wound dressing for endoscopic treatments. Acta Biomater., 159, 83-94 (2023).
- A. Nishiguchi*, T. Taguchi*, Engineering thixotropic supramolecular gelatin-based hydrogel as an injectable scaffold for cell transplantation. Biomed. Mater., 18, 015012 (2023).
2022
- K. Nagasaka, S. Watanabe, S. Ito, H. Ichimaru, A. Nishiguchi, H. Otsuka, T. Taguchi*, Enhanced burst strength of catechol groups-modified Alaska pollock-derived gelatin-based surgical adhesive. Colloids Surf. B., 220, 112946 (2022).
- A. Nishiguchi*, S. Ito, K. Nagasaka, T. Taguchi*, Liquid-liquid phase-separated hydrogel with tunable sol-gel transition behavior for hotmelt-adhesive postoperative barrier. ACS Appl. Bio Mater., 5, 4932–4941 (2022).
- S. Ito, A. Nishiguchi, H. Ichimaru, K. Nagasaka, H. Hirade, T. Taguchi*, Prevention of postoperative adhesion with a colloidal gel based on decyl group modified Alaska pollock gelatin microparticles. Acta Biomater., 149, 139-149 (2022).
- A. Nishiguchi*, H. Ichimaru, S. Ito, K. Nagasaka, T. Taguchi*, Hotmelt tissue adhesive with supramolecularly-controlled sol-gel transition for preventing postoperative abdominal adhesion. Acta Biomater., 146, 80-93 (2022).
- H. Hayasaka, J. Yoshida, Y. Kuroda, A. Nishiguchi, M. Matsusaki, K. Kishimoto, Y. Shimomura, M. Okada, D. Kobayashi, Y. Shimazu, T. Aoba, M. Akashi, M. Miyasaka*, CXCL12 promotes CCR7 ligand-guided breast cancer cell invasion and migration towards lymphatic vessels. Cancer Sci., 113, 1338-1351 (2022).
- M. Nakamoto, M. Noguchi, A. Nishiguchi, J. F. Mano, M. Matsusaki*, M. Akashi*, Fabrication of highly stretchable hydrogel based on crosslinking between alendronates functionalized poly-γ-glutamate and calcium cations, Mater. Today Bio, 14, 100225 (2022).
2021
- S. Vedaraman, A. P. Tirado, T. Haraszti, J. Gerardo-Nava, A. Nishiguchi, L. De Laporte*, Anisometric microstructures to determine minimal critical physical cues required for neurite alignment. Adv. Healthc. Mater., 10, 2100874 (2021).
- A. Nishiguchi*, T. Taguchi*, A pH-driven genipin gelator to engineer decellularized extracellular matrix-based tissue adhesives. Acta Biomater., 131, 211-221 (2021).
- P. Jain, A. Nishiguchi, G. Linz, M. Wessling, A. Ludwig, R. Rossaint, M. Möller, S. Singh*, Reconstruction of ultra-thin alveolar-capillary basement membrane mimics. Adv. Biol., 5, 2000427 (2021).
- A. Nishiguchi*, T. Taguchi*, Oligoethyleneimine-conjugated hyaluronic acid modulates inflammatory responses and enhances therapeutic efficacy for ulcerative colitis. Adv. Funct. Mater., 31, 2100548 (2021).
- S. Ito, A. Nishiguchi, F. Sasaki, H. Maeda, M. Kabayama, A. Ido, T. Taguchi*, Robust closure of post-endoscopic submucosal dissection perforation by microparticle-based wound dressing. Mater. Sci. Eng. C, 123, 111993 (2021).
- H. Ichimaru, Y. Mizuno, X. Chen, A. Nishiguchi, T. Taguchi*, Prevention of pulmonary air leaks using a biodegradable tissue-adhesive fiber sheet based on Alaska pollock gelatin modified with decanyl groups. Biomater. Sci., 9, 861-873 (2021).
- H. Maeda, F. Sasaki, Y. Morinaga, M. Kabayama, H. Iwaya, Y. Komaki, S. Arima, Y. Nasu, S. Tanoue, S. Hashimoto, S. Kanmura, A. Nishiguchi, T. Taguchi, A. Ido*, Covering post-endoscopic submucosal dissection ulcers in miniature swine with hexanoyl (Hx:C6) group-modified alkaline-treated gelatin porous film (HAG) induces proper healing by decreasing inflammation and fibrosis. Digestion, 102, 415-427 (2021).
- S. Masuda, T. Suzuki*, S. Shibata, N. Moritoki, Y. Abe, X. Chen, Y. Mizuno, A. Nishiguchi, H. Kimura, N. Matsumura, T. Iwamoto, T. Taguchi*, M. Matsumoto, M. Nakamura, A novel Alaska pollock gelatin sealant shows higher bonding strength and comparable nerve regeneration than fibrin sealant in a cadaveric model and a rat model. Plast. Reconst. Surg., 148, 742e-752e (2021).
2020
- A. Nishiguchi*, T. Taguchi*, Engineering injectable tough tissue adhesive through nanocellulose reinforcement. ACS Appl. Bio Mater., 3, 9093-9100 (2020).
- S. Singh, Y. Marquardt, R. Rimal, A. Nishiguchi, S. Huth, M. Akashi, M. Möller, J. M. Baron*, Long-term and clinically relevant full thickness human skin equivalent for psoriasis. ACS Appl. Bio Mater., 3, 6639–6647 (2020).
- A. Nishiguchi*, T. Taguchi*, Development of an immunosuppressive camouflage-coating platform with nanocellulose and cell membrane vesicles. J. Biomater. Sci. Polym. Ed., 15, 1912-1924 (2020).
- X. Chen, A. Nishiguchi, T. Taguchi*, Adhesive submucosal injection material based on the nonanal group-modified poly(vinyl alcohol)/α-cyclodextrin inclusion complex for endoscopic submucosal dissection. ACS Appl. Bio Mater., 3, 4370-4379 (2020).
- A. Nishiguchi, G. Kapiti, J. R. Höhner, S. Singh, M. Möller*, In situ 3D-printing using a bio-ink of protein-photosensitizer conjugates for single cell manipulation. ACS Appl. Bio Mater., 3, 2378-2384 (2020).
- A. Nishiguchi, F. Shima, S. Singh, M. Akashi, M. Möller*, 3D-printing of structure-controlled antigen nanoparticles for vaccine delivery. Biomacromolecules, 21, 2043–2048 (2020).
- A. Nishiguchi, Y. Kurihara, T. Taguchi*, Hemostatic, tissue-adhesive colloidal wound dressing functionalized by UV irradiation. ACS Appl. Bio Mater., 3, 1705−1711 (2020).
- A. Nishiguchi, H. Zhang, S. Schweizerhof, M. F. Schulte, A. Mourran, M. Möller*, 4D-printing of light-driven soft actuator with programmed printing density. ACS Appl. Mater. Interfaces, 12, 12176−12185 (2020).
- A. Nishiguchi*, T. Taguchi*, A thixotropic, cell-infiltrative nanocellulose hydrogel that promotes in vivo tissue remodeling. ACS Biomater. Sci. Eng., 6, 946−958 (2020).
- A. Nishiguchi*, T. Taguchi*, Sustained-immunostimulatory nanocellulose scaffold to enhance vaccine efficacy. J. Biomed. Mater. Res. A, 108, 1159–1170 (2020).
- A. Nishiguchi, T. Taguchi*, Designing an anti-inflammatory and tissue-adhesive colloidal dressing for wound treatment. Colloid Surf. B., 188, 110737 (2020).
2019
- M. O50. A. Nishiguchi, Y. Kurihara, T. Taguchi*, Underwater-adhesive microparticle dressing composed of hydrophobically-modified Alaska pollock gelatin for gastrointestinal tract wound healing. Acta Biomater., 99, 387-396 (2019).
- A. Nishiguchi, F. Sasaki, H. Maeda, M. Kabayama, A. Ido, T. Taguchi*, Multi-functional hydrophobized microparticles for accelerated wound healing after endoscopic submucosal dissection. Small, 15, 1901566 (2019).
- A. Nishiguchi*, T. Taguchi*, Osteoclast-responsive, injectable bone of bisphosphonated-nanocellulose that regulates osteoclast/osteoblast activity for bone regeneration. Biomacromolecules, 20, 1385-1393 (2019).
- A. Nishiguchi, C. Gilmore, A. Sood, M. Matsusaki, G. Collett, D. Tannetta, I.L. Sargent, J. McGarvey, N.D. Halemani, J. Hanley, F. Day, S. Grant, C. Murdoch-Davis, H. Kemp, P. Verkade, J.D. Aplin, M. Akashi*, C.P. Case, In vitro placenta barrier model using primary human trophoblasts, underlying connective tissue and vascular endothelium. Biomaterials, 192, 140-148 (2019).
- S. Iwai, S. Kishimoto, Y. Amano, A. Nishiguchi, M. Matsusaki, A. Takeshita, M. Akashi*, Three-dimensional cultured tissue constructs that imitate human living tissue organization for analysis of tumor cell invasion. J. Biomed. Mater. Res. Part A, 107, 292-300 (2019).
2018
- A. Nishiguchi, M. Matsusaki, M.R. Kano, H. Nishihara, D. Okano, Y. Asano, H. Shimoda, S. Kishimoto, S. Iwai, M. Akashi*, In vitro 3D blood/lymph-vascularized human stromal tissues for preclinical assays of cancer metastasis. Biomaterials, 179, 144-155 (2018).
- A. Nishiguchi, A. Mourran, H. Zhang, M. Möller*, In-gel direct laser writing for 3D-designed hydrogel composites that undergo complex self-shaping. Adv. Sci., 5, 1700038 (2018).
- E. Dohle, S. Singh, A. Nishiguchi, T. Fischer, M. Wessling, M. Möller, R. Sader, J. Kasper, S. Ghanaati, C.J. Kirkpatrick*, Human co- and triple-culture model of the alveolar-capillary barrier on a basement membrane mimic. Tissue Eng. Part C, 24, 495-503 (2018).
2017
- A. Nishiguchi, S. Singh, C.J. Kirkpatrick, M. Möller*, Basement membrane mimetics of biofunctionalized nanofibers for a bipolar-cultured human primary alveolar-capillary barrier model. Biomacromolecules, 18, 719−727 (2017).
2016
- V. Gribova, C.-Y. Liu, A. Nishiguchi, M. Matsusaki, T. Boudou, C. Picart, M. Akashi*, Construction and myogenic differentiation of 3D myoblast tissues fabricated by fibronectin-gelatin nanofilm coating. Biophys. Biochem. Res. Commun., 3, 515-521 (2016).
- D. Hikimoto, A. Nishiguchi, M. Matsusaki, M. Akashi*, High-throughput blood- and lymph-capillaries with open-ended pores which allow the transport of drugs and cells. Adv. Healthc. Mater., 5, 1969-1978 (2016).
- Y. Amano, T. Igarashi, A. Nishiguchi, M. Matsusaki, Y. Saito, K. Nakamura, H. Ito, M. Akashi*, Construction of mES derived 3D-pacemaker tissues by layer-by-layer nanofilm coating. ChemNanoMat, 2, 466–471 (2016).
- Y. Amano, A. Nishiguchi, M. Matsusaki, H. Iseoka, S. Miyagawa, Y. Sawa, M. Seo, T. Yamaguchi, M. Akashi*, Development of vascularized iPSC derived 3D-cardiac myoblast tissues by filtration layer-by-layer technique and their application for pharmaceutical assays. Acta Biomater., 15, 110-121 (2016).
- N. Uchida, S. Sivaraman, N.J. Amoroso, W.R. Wagner, A. Nishiguchi, M. Matsusaki, M. Akashi, J. Nagatomi*, Nanometer-sized extracellular matrix coating on polymer-based scaffold for tissue engineering. J. Biomed. Mater. Res. Part A, 104, 94-103 (2016).
2015
- A. Nishiguchi, M. Matsusaki, M. Akashi*, Structural and viscoelastic properties of layer-by-layer ECM nanofilms and their interactions with living cells. ACS Biomater. Sci. Eng., 1, 816-824 (2015).
- A. Nishiguchi, M. Matsusaki, S. Miyagawa, Y. Sawa, M. Akashi*, Dynamic nano-interfaces enable harvesting of functional 3D-engineered tissues. Adv. Healthc. Mater., 4, 1164-1168 (2015).
- A. Nishiguchi, M. Matsusaki, M. Akashi*, Cell-cell crosslinking by bio-molecular recognition of heparin-based layer-by-layer nanofilms. Macromol. Biosci., 15, 312-317 (2015) (Selected as a front cover).
- K. Uesugi, A. Nishiguchi, M. Matsusaki, M. Akashi, K. Morishima*, Evaluation system for mechanobiology of three-dimensional tissue multilayered in vitro. 2015 Int. Symp. Micro-Nano Mechatronics Human Sci., 7438345 (2015).
- M. Matsusaki, D. Hikimoto, A. Nishiguchi, K. Kadowaki, K. Ohura, T. Imai, M. Akashi*, 3D-fibroblast tissues constructed by a cell-coat technology enhance tight-junction formation of human colon epithelial cells. Biochem. Biophys. Res. Commun., 457, 363-369 (2015).
2014
- D. Curtis, A. Sood, T. Phillips, V. Leinster, A. Nishiguchi, C. Coyle, L. Lacharme-Lora, O. Beaumont, H. Kemp, R. Goodall, L. Cornes, M. Giugliano, R. Barone, M. Matsusaki, M. Akashi, H. Y. Tanaka, M. Kano, J. McGarvey, N. D. Halemani, K. Simon, R. Keehan, W. Ind, T. Masters, S. Grant, S. Athwal, G. Collett, D. Tannetta, I. L. Sargent, E. Scull-Brown, X. Liu, K. Aquilina, N. Cohen, J. D. Lane, M. Thoresen, J. Hanley, A. Randall, C. P. Case*, Secretions from placenta, after hypoxia/reoxygenation, can damage developing neurones of brain under experimental conditions. Exp. Neurol., 261, 386-395 (2014).
- A. Nishiguchi, M. Matsusaki, Y. Asano, H. Shimoda, M. Akashi*, Effects of angiogenic factors and 3D-microenvironments on vascularization within sandwich cultures. Biomaterials, 35, 4239-4748 (2014).
- Y. Asano, A. Nishiguchi, M. Matsusaki, D. Okano, E. Saito, M. Akashi, H. Shimoda*, Ultrastructure of blood and lymphatic vascular networks in three-dimensional cultured tissues fabricated by extracellular matrix nanofilm-based cell accumulation technique. Microscopy, 63, 219-226 (2014).
2012
- J. Sasaki, T. Matsumoto, H. Egusa, M. Matsusaki, A. Nishiguchi, T. Nakano, M. Akashi, S. Imazato, H. Yatani*, In vitro reproduction of endochondral ossification using a 3D mesenchymal stem cell construct. Integr. Biol., 4, 1207-1214 (2012).
2011
- A. Nishiguchi, H. Yoshida, M. Matsusaki, M. Akashi*, Rapid construction of three-dimensional multilayered tissues with endothelial tube networks by the cell-accumulation technique. Adv. Mater., 23, 3506-3510 (2011).
2010
- A. Nishiguchi, H. Yoshida, M. Matsusaki, M. Akashi*, Preparation of reduction-sensitive nanogels with a large swelling capacity by a surfactant-free precipitation method. Chem. Lett., 39, 1184-1185 (2010).
解説・総説・著書
- 西口昭広、田口哲志、月刊バイオインダストリー、相分離を利用した多孔性組織接着剤の設計、2025年
- 西口昭広、安江 華、田口哲志、界面制御による革新的生体適合性材料の開発最前線、液-液相分離制御技術を用いた多孔化インジェクタブルゲルの開発、第5章1節、361-372、2025年
- 小松ひより、西口昭広、田口哲志、バイオマテリアル―生体材料―、生体内での膨潤特性を制御した天然高分子由来組織接着性ハイドロゲルの設計と脳硬膜閉鎖への応用、43-3、214-219、2025年
- 西口昭広、バイオマテリアル―生体材料―、日本バイオマテリアル学会、液-液相分離制御によるインジェクタブルゲルの開発、43-1、18-19、2025年
- 西口昭広、田口哲志、組織接着剤、ハイドロゲルの特性と作製および医療材料への応用、R&D支援センター、第3節、66-73、2024年
- 伊藤椎真、西口昭広、田口哲志、生体吸収性外科材料の使い方と新しい材料の有用性、技術情報協会、穿孔閉鎖能と癒着防止能を有する創傷被覆粒子の開発、第6節、294、2024年
- 西口昭広、田口哲志、Drug Delivery System、日本DDS学会、生体機能化ポリマーによる免疫細胞機能制御、38、379-387、2023年
- 西口昭広、田口哲志、Material Stage、技術情報協会、ゾル-ゲル転移制御に基づくホットメルト型医療用接着剤の開発と癒着防止材への応用、23、35-40、2023年
- 西口昭広、田口哲志、バイオマテリアル―生体材料―、日本バイオマテリアル学会、組織接着性ハイドロゲルの設計と術後合併症予防への応用、41-2、102-104、2023年
- 西口昭広、田口哲志、バイオマテリアル―生体材料―、日本バイオマテリアル学会、ゾル-ゲル転移制御によるホットメルト組織接着剤の創出、41、68-69、2023年
- 西口昭広、田口哲志、月刊BIO INDUSTRY、シーエムシー出版、術後合併症を予防するホットメルト組織接着剤開発、39、22-27、2022年
- 西口昭広、伊藤椎真、田口哲志、J. Jpn. Soc. Colour Mater.、色材協会、組織接着性バイオポリマー微粒子の設計と医療応用、95, 341-345、2022年
- 伊藤椎真、西口昭広、田口哲志、製品開発に向けたバイオマテリアル開発の基本事項と注意点、情報機構、早期消化管がん除去後の穿孔を閉鎖する組織接着性粒子の設計、第6節、273-281、2022年
- 西口昭広、田口哲志、人工臓器、日本人工臓器学会、組織接着性バイオマテリアルの開発、50、199-202、2021年
- 西口昭広、田口哲志、WEBジャーナル、有限会社アクトライエム、ナノセルロース強化組織接着剤の開発、9、9-13、2021年
- 西口昭広、田口哲志、Drug Delivery System、日本DDS学会、がん微小環境体外モデル構築のためのバイオマテリアル開発、36、256-264、2021年
- 西口昭広、田口哲志、日本接着学会誌、日本接着学会、疎水化技術に基づく生体組織接着性粒子の開発と医療応用、総合論文、57、220-226、2021年
- 西口昭広、田口哲志、月刊せんい、日本繊維機械学会、生分解性セルロースナノファイバーを用いた機能性足場材料の開発、74、33-39、2021年
- 西口昭広、田口哲志、バイオマテリアル―生体材料―、日本バイオマテリアル学会、消化管がん治療に向けた組織接着性創傷被覆粒子の開発、39巻、18-19、2021年
- 西口昭広、Precision Medicine、再生医療のためのバイオマテリアル、北隆館、3、55-60、2020年
- 西口昭広、田口哲志、WEB Journal、有限会社アクトライエム、ナノセルロースを用いた整形外科用バイオマテリアルの開発、25、7-10、2019年
- 西口昭広、田口哲志、化学装置、工業通信、ナノセルロースを用いた機能性バイオマテリアルの開発、61、27-32、2019年
- 水野陽介、水田 亮、西口昭広、田口哲志、人工臓器、日本人工臓器学会、湿潤組織に対するシーリング効果を示す疎水化タラゼラチン接着剤の創製、47、39、2018年
- 水田 亮、西口昭広、田口哲志、高分子、高分子学会、強度と生体親和性を両立する革新的外科用接着剤、66、490-493、2017年
- 浅野義哉、松﨑典弥、岡野大輔、西口昭広、明石満、下田浩、リンパ学、日本リンパ学会、細胞集積法によるヒト人工三次元脈管組織のエンジニアリングと移植、39、18-20、2016年
- 西口昭広、松崎典弥、明石 満、 三次元ティッシュエンジニアリング、NTS、細胞外マトリックスのレイヤーバイレイヤーによる組織構築、2、281-291、2015年
- 西口昭広、松崎典弥、明石 満、月刊バイオインダストリー、シーエムシー出版、バイオファブリケーション~機械で臓器を作る~、Layer by Layer細胞コーティング法~マテリアル技術からのアプローチ~、31、28-36、2014年
- A. Nishiguchi, M. Matsusaki, M. Akashi, Engineered Cell Manipulation for Biomedical Application, Springer-Verlag, The Potential Use of Three-Dimensional Cellular Multilayers as a Blood Vessel Model, VIII, 271, 93 (2014)
- 西口昭広、明石 満、未来型人工関節を目指して―その歴史から将来展望まで―、日本医学館、第1編、第5章、2-4、石灰化促進のための高分子材料、206-211、2013年
- 松崎典弥、西口昭広、狩野光伸、明石満、再生医療、日本再生医療学会、毛細血管網を含む創傷部モデルを用いたIn vitro癌細胞浸潤試験による血管網への影響評価、12、163、2013年
- 松崎典弥、門脇功治、西口昭広、明石 満、日本生理学雑誌、日本生理学会、細胞積層技術による生体外での血管モデルの構築と血管機能評価への応用、74(5)、250-251、2012年
- 松崎典弥、パニニー チャーパユーン、西口昭広、明石 満、科学と工業、大阪工研協会、高分子ナノ薄膜を用いた細胞表面の制御に基づく細胞積層技術、86(9)、318-324、2012年
- 松崎典弥、西口昭広、門脇功治、明石 満、ナノ融合による先進バイオデバイス、シーエムシー出版、第1編 第3章 4 ナノ薄膜による細胞の三次元操作、123-132、2011年
Project
競争的資金
- 1. 創発的研究支援事業(2025年10月-2029年3月)
相分離材料学が拓く細胞移植ゲルによる組織再生(JPMJFR244T) - 2. 上原記念生命科学財団・研究助成(2025年1月-2026年3月)
多孔化インジェクタブルゲルによる細胞移植法の創出 - 3. 小笠原敏晶記念財団・一般研究助成(2025年1月-2026年12月)
液-液相分離誘導技術による構造制御インジェクタブルゲルの開発 - 4. 泉科学技術振興財団・研究助成(2024年10月-2026年9月)
組織リモデリングを促進する超分子血管塞栓剤の創出と画像下治療への応用 - 5. 科研費・挑戦的研究(萌芽)(2024年9月-2026年3月)
ゲノム編集スキャフォールドによるin vivoダイレクトリプログラミング - 6. AMED・橋渡し研究戦略的推進プログラム・シーズA(2024年4月-2026年3月)
組織再生を促進する多孔性フォトグルーの開発 - 7. 稲盛財団・稲盛研究助成(2024年4月-2026年3月)
液-液相分離制御によるin vivo血管化技術の開発 - 8. 科研費・挑戦的研究(萌芽)(2022年9月-2024年3月)
ポリアミンナノ粒子による腸管微小環境ネットワークの制御と炎症性腸疾患治療への応用(22K19947) - 9. 科研費・基盤B(2022年4月-2026年3月)
ゾル-ゲル転移制御に基づくホットメルト組織接着剤の開発(22H03962、23K25216) - 10. 上原記念生命科学財団・研究奨励金(2022年1月-2023年3月)
1液型超分子インジェクタブルゲルによる組織再生 - 11. 科研費・若手研究(2020年4月-2022年3月)
免疫拒絶反応を抑制する再生医療用スキャフォールドの創出(20K20207) - 12. AMED・橋渡し研究戦略的推進プログラム・シーズA(2020年4月-2022年3月)
炎症性疾患治療に向けた抗炎症ポリアミンナノ粒子の開発(JP20lm0203010) - 13. 科研費・若手研究(2018年4月-2020年3月)
ナノバイオ界面機能を制御する疎水化微粒子を用いた創傷治癒促進材料の開発(18K14099)
CV of PI

| 2010年3月 | 大阪大学工学部応用自然科学科応用化学コース 卒業 |
|---|---|
| 2012年3月 | 大阪大学大学院工学研究科応用化学専攻 修士課程修了 |
| 2015年3月 | 大阪大学大学院工学研究科応用化学専攻 博士課程修了 博士(工学)(大阪大学) |
| 2015年4月~ 2017年1月 |
DWI-Leibniz Institute for Interactive Materials 博士研究員 |
| 2017年2月~ 2020年3月 |
(国研)物質・材料研究機構 機能性材料研究拠点 研究員 |
| 2020年4月~ 2023年3月 |
(国研)物質・材料研究機構 機能性材料研究拠点 主任研究員 |
| 2023年4月~ 現在 |
(国研)物質・材料研究機構 高分子・バイオ材料研究センター 主幹研究員 |
| 2024年4月~ 現在 |
東京理科大学大学院 先進工学研究科 マテリアル創成工学専攻 客員准教授 |
| 2026年4月~ 現在 |
筑波大学大学院 理工情報生命学術院 数理物質系 准教授 (応用理工学学位プログラム/NIMS連係物質・材料工学サブプログラム) |
| 2025年10月~ 現在 |
JST 創発研究者 |
受賞
- 令和7年度文部科学大臣表彰 若手科学者賞、高分子間相互作用制御による組織再生ハイドロゲル開発の研究、2025年4月15日
- バイオマテリアル科学奨励賞(日本バイオマテリアル学会)、液-液相分離制御によるインジェクタブルゲルの開発、2024年10月29日
- 高分子研究奨励賞(2022年、高分子学会)、生体組織接着性ハイドロゲルの開発と術後合併症予防への応用、2023年5月25日
- 日韓バイオマテリアル学会若手研究者交流AWARD(日本バイオマテリアル学会)、消化管がん治療に向けた組織接着性創傷被覆粒子の開発、2020年11月
- 日本接着学会奨励賞(2020年、日本接着学会)、生体組織接着を実現する疎水化微粒子の設計と創傷被覆材への応用、2020年6月13日
所属学会
- 高分子学会(正会員、医用高分子研究会)
- 日本バイオマテリアル学会(正会員、評議員)
- 日本接着学会(正会員、評議員)
- 日本人工臓器学会(正会員、評議員)
- 日本再生医療学会
- 日本DDS学会(正会員、DDS編集幹事)
- Editorial Board Member, Tissue Engineering Pat C: Methods, Jan 2024~
報道
- 温めて塗るだけで傷を治す医療用接着剤、JETI、2022年9月22日
- 医療用ホットメルト接着剤―体温付近で高い強度、化学工業日報、2022年7月25日
- 手術の癒着、新接着剤で防止、日本経済新聞、26面、2022年5月29日
- プレスリリース、温めて塗るだけで傷を治す医療用接着剤を開発~ホットメルト特性で術後合併症をクールに予防~国立研究開発法人物質・材料研究機構、2022年5月19日
- がん手術後の炎症抑える被覆材開発、毎日新聞、16面、2019年10月2日
- プレスリリース、がん手術後の炎症を抑える粒子状の被覆材を開発~ブタゼラチン疎水化で接着力が大幅向上、内視鏡で噴霧も可能に 深刻な偶発症の予防へ前進~、国立研究開発法人物質・材料研究機構、国立大学法人 鹿児島大学、2019年7月30日
Contact
西口研究室
国立研究開発法人物質・材料研究機構 高分子・バイオ材料研究センター バイオ材料分野 バイオポリマーグループ
筑波大学大学院 理工情報生命学術院 数理物質系
東京理科大学大学院 先進工学研究科 マテリアル創成工学専攻
Tel. 029-860-4987Tel. 029-860-4987 Fax. 029-860-4752
E-mail: NISHIGUCHI.Akihiro[at]nims.go.jp