薬物送達システム(DDS:Drug Delivery System)は薬物を必要な時に必要なだけ病巣に輸送するシステムです。体内で薬物を少しずつ一定量徐放する放出制御と病巣に薬物を輸送する標的化に区別されます。特に人体に強い作用を及ぼす薬物(例えば抗癌剤など)を投与すると、直後に薬物の効果が過剰に発現または他の部位へ移行して副作用を発現し、患者に多大な苦痛を与えてしまいます。そのため、私達の身体への副作用を低減させ、その効能・効果を最大限に発揮させることが求められています。プロテオーム技術(特定の細胞や組織が作り出す全てのタンパク質に関する解析技術)や遺伝子解析技術などの進展に伴い、沢山の有用なタンパク製剤の開発が進められてきています。一般にタンパク質は水溶液中で不安定であるため、その安定化・徐放化・持続化が研究開発の課題です。リン酸カルシウムである水酸アパタイトは骨の無機主成分であり、骨充填材などとして既に臨床応用されている生体に安全な材料です。また、液体クロマトグラフィーなどのカラム充填材として用いられ、タンパク質の工業的な分離・精製などの工程に利用されています。
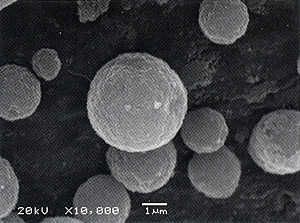
私達は図1に示す走査型電子顕微鏡像のように1〜10μmの球形の多孔質微粒子を作製しています。比表面積が90〜180m2 /gと市販されている水酸アパタイト微粒子と比較して約2倍程度の大きな値を示します。図2に微粒子を100nm以下の厚さに切り取った断面の透過型電子顕微鏡像を示します。水酸アパタイトがナノ結晶であること、さらに10〜100nmの細孔が空いていることが分かります。結晶の大きさ・比表面積を制御することで従来と比較して1.5倍以上のタンパク質を吸着させることができます。また、細孔の「ナノ空間」を利用してタンパク質を結晶化させる技術開発を行っています。微粒子の開発・タンパク質の結晶化技術などを複合化させることで、1〜2週間安定にタンパク質を生体内で徐放させることが可能です。今後、さらに安定性・徐放性を改善することでより安全な担体材料開発を目指します。 |